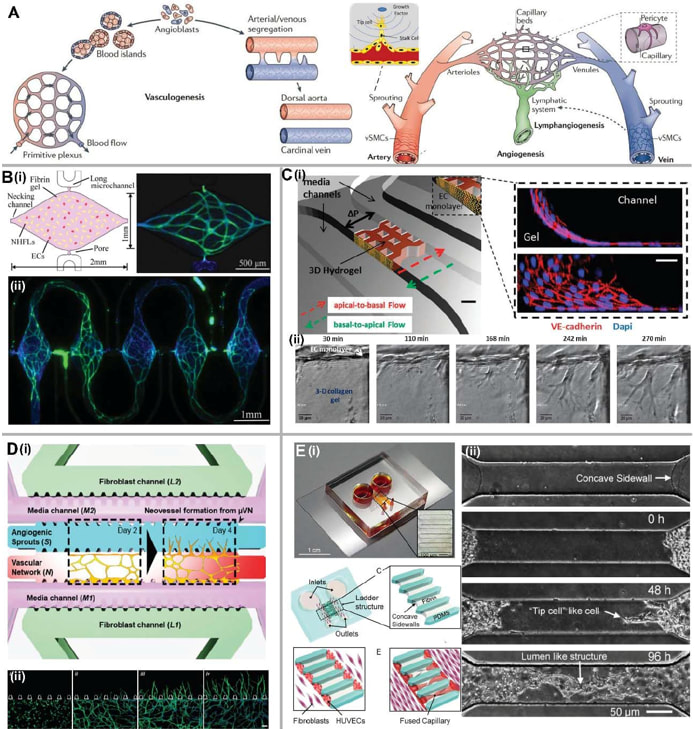
血管生成(vasculogenesis)和血管新生(angiogenesis)是体内血管发育的重要过程,如图1A所示。在早期胚胎发育期间,血管生成促进原始血管丛的形成,而血管新生决定着血管网络的丰富和扩张。在成人中,新血管的形成可以来自骨髓中的内皮细胞。同样地,在某些生理和病理条件下(如伤口愈合、运动和肿瘤生长),来自组织的应激信号可以刺激并促使血管新生。与上一部分中提到的EC内衬相比较,血管生成和血管新生不需要微结构引导EC形成血管,二者允许ECM内接种的细胞自发生成3D微血管网络,因此,该方法可以重构更加自然、真实的血管结构。
1)血管生成(Vasculogenesis)
血管生成是指内皮祖细胞(EPCs)最初形成新血管的过程。在微流控装置中,Hsu等人证明了将由细胞源性内皮细胞(ECFC-ECs)和正常人肺成纤维细胞(NHLF)混合在纤维蛋白凝胶内,并灌注进多个菱形组织室中,最终形成微血管网络(图1B)。在一定范围的间隙流速内,即使没有血管内皮生长因子(VEGF)和碱性成纤维细胞生长因子(bFGF),通过灌注细胞培养基,大约三周后便可形成连续的可灌注血管网络。据报道,血管化组织可以培养并存活40天,但随时间的推移可能终止并脱落。此外,来自成纤维细胞蛋白的互相结合有利于促进EC的萌发,这对血管腔的生成十分重要。作为化学因子,VEGF和bFGF也可来刺激血管生成。Raghavan等人提出了一种控制血管几何形态的方法,该方法是通过在凝胶内将EC分布式图案化,证明了VEGF和bFGF刺激24-48h内可形成管腔。利用该方法,通过改变凝胶浓度及接种细胞密度,可得到直径、形状不同的微血管。结果表明,随着纤维蛋白原浓度的增加,血管平均分枝长度和有效直径均减小,但血管分枝长度、直径和面积占比均随EC接种密度的增加而提升。除此之外,与其他类型细胞共培养的旁分泌信号也会影响血管形态,如血管分枝数、平均分支长度、血管化面积百分比和平均血管直径等。在与成纤维细胞共培养的条件下,血管网络覆盖面积增大,而在促血管生长因子的作用下,血管直径和平均血管长度降低。其他基质细胞如周细胞、SMC或间充质干细胞(MSCs)也能提高生成血管的稳定程度,这些为在体外构建特定形态的微血管网络提供了调节机制。
2)血管新生(Angiogenesis)
血管新生是指在原有血管的基础上形成新的血管,是血管网络重构的重要机制。血管新生需经过一系列过程,包括基质金属蛋白酶(MMPs)降解ECM、血管生成刺激、出芽、伸长和分支、管腔形成、吻合、最终稳定或凋亡。在微流控装置中,血管生成可由EC内衬的微血管或已有的微血管网络诱导。研究发现,伴随细胞连接和肌动蛋白细胞骨架的重新分布,激酶介导的信号传导对内皮血管芽的生成有一定影响(图1C)。此外,VEGF梯度同样能诱导EC的血管新生。此前,Kim等人提出了一种3D体外模型,研究了在间隙流刺激下从已有的微血管网络中产生新的血管芽(图1D)。结果发现,血管新生芽仅在与间隙流相反的方向上被促进生成,而在其流动方向上被抑制。
为构建可灌注的微血管网络,血管新生芽要通过称为血管吻合(anastomosis)的过程相互连接。Yeon等人将HUVEC排列在纤维蛋白凝胶的两旁侧壁上,通过与NHLF共培养,血管新生芽在3-4天的刺激后融合在一起(图1E)。在微加工制程中,通过调节限制ECM的微结构间距,可以理想控制血管新生芽的间距。类似地,Song等人提出的器件能够准确地再现VEGF作用下血管吻合的过程。这些微流控装置为研究血管新生机制和药物筛选提供了新颖、实用的平台。
1)血管生成(Vasculogenesis)
血管生成是指内皮祖细胞(EPCs)最初形成新血管的过程。在微流控装置中,Hsu等人证明了将由细胞源性内皮细胞(ECFC-ECs)和正常人肺成纤维细胞(NHLF)混合在纤维蛋白凝胶内,并灌注进多个菱形组织室中,最终形成微血管网络(图1B)。在一定范围的间隙流速内,即使没有血管内皮生长因子(VEGF)和碱性成纤维细胞生长因子(bFGF),通过灌注细胞培养基,大约三周后便可形成连续的可灌注血管网络。据报道,血管化组织可以培养并存活40天,但随时间的推移可能终止并脱落。此外,来自成纤维细胞蛋白的互相结合有利于促进EC的萌发,这对血管腔的生成十分重要。作为化学因子,VEGF和bFGF也可来刺激血管生成。Raghavan等人提出了一种控制血管几何形态的方法,该方法是通过在凝胶内将EC分布式图案化,证明了VEGF和bFGF刺激24-48h内可形成管腔。利用该方法,通过改变凝胶浓度及接种细胞密度,可得到直径、形状不同的微血管。结果表明,随着纤维蛋白原浓度的增加,血管平均分枝长度和有效直径均减小,但血管分枝长度、直径和面积占比均随EC接种密度的增加而提升。除此之外,与其他类型细胞共培养的旁分泌信号也会影响血管形态,如血管分枝数、平均分支长度、血管化面积百分比和平均血管直径等。在与成纤维细胞共培养的条件下,血管网络覆盖面积增大,而在促血管生长因子的作用下,血管直径和平均血管长度降低。其他基质细胞如周细胞、SMC或间充质干细胞(MSCs)也能提高生成血管的稳定程度,这些为在体外构建特定形态的微血管网络提供了调节机制。
2)血管新生(Angiogenesis)
血管新生是指在原有血管的基础上形成新的血管,是血管网络重构的重要机制。血管新生需经过一系列过程,包括基质金属蛋白酶(MMPs)降解ECM、血管生成刺激、出芽、伸长和分支、管腔形成、吻合、最终稳定或凋亡。在微流控装置中,血管生成可由EC内衬的微血管或已有的微血管网络诱导。研究发现,伴随细胞连接和肌动蛋白细胞骨架的重新分布,激酶介导的信号传导对内皮血管芽的生成有一定影响(图1C)。此外,VEGF梯度同样能诱导EC的血管新生。此前,Kim等人提出了一种3D体外模型,研究了在间隙流刺激下从已有的微血管网络中产生新的血管芽(图1D)。结果发现,血管新生芽仅在与间隙流相反的方向上被促进生成,而在其流动方向上被抑制。
为构建可灌注的微血管网络,血管新生芽要通过称为血管吻合(anastomosis)的过程相互连接。Yeon等人将HUVEC排列在纤维蛋白凝胶的两旁侧壁上,通过与NHLF共培养,血管新生芽在3-4天的刺激后融合在一起(图1E)。在微加工制程中,通过调节限制ECM的微结构间距,可以理想控制血管新生芽的间距。类似地,Song等人提出的器件能够准确地再现VEGF作用下血管吻合的过程。这些微流控装置为研究血管新生机制和药物筛选提供了新颖、实用的平台。