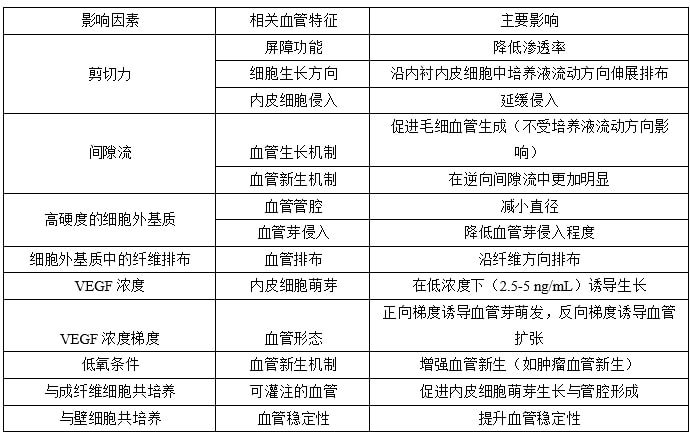
由于在生理水平上能够精确控制微环境中的流体流动、化学因子的分布以及细胞外基质特性(如硬度、取向等)等方面的优势,微流控系统已成为体外培养微血管的新兴工具。诱导因素可分为三大类:生物力学因素、细胞外(或扩散)信号分子、细胞源和细胞间相互作用。下表总结了影响不同血管参数的主要因素。
1)生物力学因素
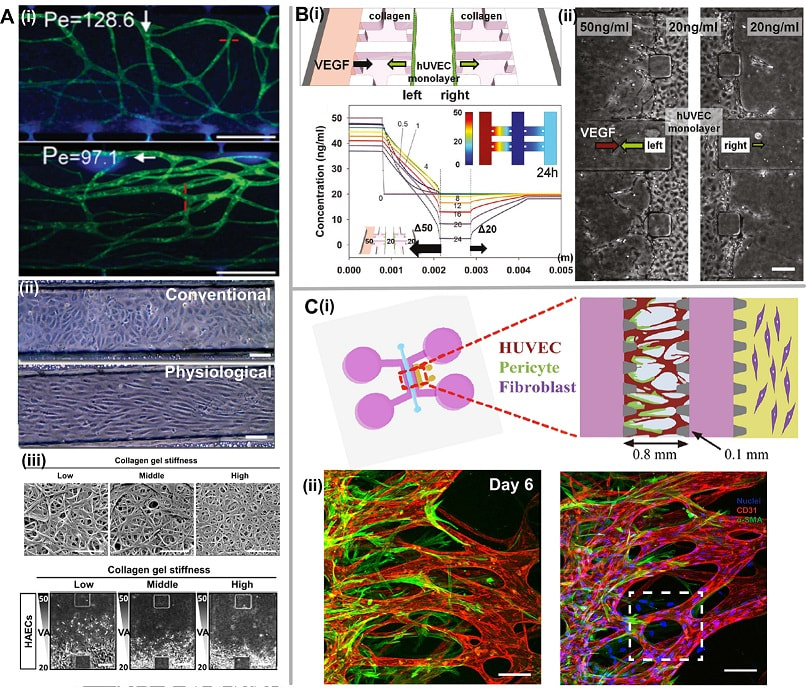
在微流控器件中,生物力学因素是流体通过微流控通道或细胞外基质(ECM)产生的不同应力。剪切力是主要的生物力学因素,它高度依赖于流体流动。研究发现,剪切应力通过降低血管通透性以及降低血管壁厚度来增强屏障功能。对于EC内衬,EC在剪切力作用下被拉长并与流动方向对齐(图1(Aii))。此外,剪切应力能够通过一氧化氮(NO)信号刺激减弱HUVEC的入侵,这不受间隙流方向和VEGF梯度的影响。
间隙流是调节体内外细胞行为的另一重要因素,其对EC的作用力可促进毛细血管的形成。在体内,0.1–1 μm/s范围内的间隙流可刺激血管形成。在微流控装置中,流速如果在1.7–11 μm/s范围内,并伴随着较大的Péclet数(Pe>10),无论间隙流方向如何,都可刺激血管生成(图1(Ai))。这里Péclet数为对流与扩散传输的比率。对于血管新生,在与逆着间隙流方向上,从已有的血管网络中生成新血管的行为更加明显。研究发现,从基底到顶端的跨内皮流动可以触发EC从静止表型向侵袭表型的转变,从而生成血管。
除了流体力外,凝胶渗透率、孔径、纤维直径和硬度、降解速度等ECM力学性能在调节血管生成中也发挥了重要作用。胶原蛋白(collagen)和纤维蛋白(fibrin)是最常用的天然水凝胶,其力学性能可以灵活微调。胶原的力学性能可通过改变温度或pH的变化来调节,纤维蛋白的力学性能可通过改变纤维蛋白原和凝血酶浓度来调节。结果发现,与软凝胶相比,较硬的凝胶会产生直径较小的血管腔,血管芽结构在硬胶原凝胶中的侵袭程度明显降低(图1(Aiii))。此外,ECM内的纤维排布也会影响血管分布。除了这些被动机械应力外,施加在ECM上的主动机械应力对血管也会产生影响。例如,浮动的支架会使血管随机定向分布。然而,单向结构上的循环拉伸会使血管呈对角生长,而静态拉伸使血管呈垂直形生长。
2)细胞外信号分子
生长因子是细胞分泌的物质,它能够刺激细胞生长、增殖和分化。VEGF作为最重要的生长因子,能够通过VEGF受体-2信号调节EC的迁移和增殖。研究发现,较低浓度(2.5–5 ng/ml)的VEGF可诱导EC出芽。负VEGF梯度会诱导类似血管扩张的过程,而正VEGF梯度可诱导血管芽生成。除VEGF外,其他血管生成生长因子如血管生成素1(Ang-1)、转化生长因子β1(TGF-1)和碱性成纤维细胞生长因子(bFGF)可通过内皮尖端细胞丝状伪足从低浓度向高浓度梯度引导血管生成,并形成良好的排列。因此,生长因子的浓度梯度对于组织血管化至关重要(图1B)。这可以通过将含有成纤维细胞的海藻酸钠球体或包裹生长因子的微粒嵌入水凝胶中以产生局部浓度梯度来实现,或者通过微流控装置灌注含有生长因子的细胞培养基来实现。与作用于血管网络的单一生长因子相比,多种生长因子的组合会提高血管密度和稳定性。此外,通过调节流速和设计不同的微流控结构,可以构建不同梯度的生长因子。除了生长因子的空间效应外,VEGF浓度的时间变化也会影响血管生成。研究发现,与恒定剂量的血管内皮生长因子相比,高浓度的血管内皮生长因子的初始梯度随着时间的推移逐渐降低,可诱导生成理想的血管芽。因此,生长因子的释放、组合、剂量、梯度分布以及合适的作用时间都将促进血管的形成和稳定。
除生长因子的直接影响外,氧张力也会影响VEGF的分泌。缺氧环境中分泌的缺氧诱导因子(HIF)-1可启动VEGF的转录,这在诱导抗凋亡蛋白的表达,尤其是在肿瘤血管生成等病理性血管生成模型中起着重要作用。利用微流控可产生所需的氧气微环境,比如,由于PDMS的透气性高,通入不同浓度的气体、注入气体平衡培养液、氧清除操作或生成化学物质可以灵活创造缺氧微环境和氧张力梯度。此外,通过组合低透气热塑性塑料,能抑制外部微环境的干扰,从而增强了对PDMS热塑性混合微流控装置的氧气控制。
3)细胞源与细胞之间的作用
EC是组织血管形成的主要细胞。HUVEC由于其相对简单的分离方法被广泛应用于体外血管构建。不过当需要特异性EC时,需要使用其他EC来源来代替HUVEC。此外,诱导多能干细胞(iPSCs)衍生的EC已成为个性化药物研究的新内皮细胞来源。为了在体外建立成熟稳定的血管网络,需要将内皮细胞与壁细胞(如成纤维细胞、周细胞或MSCs)共培养。成纤维细胞可以合成并维持必要的基质蛋白(如I型胶原),分泌各种血管生成生长因子,以促进EC生成血管芽并形成管腔。此外,在稳定新形成的血管方面,在毛细血管和大血管(如小动脉、动脉、小静脉和静脉)周围的周细胞和平滑肌细胞(SMCs)也发挥着重要作用(图1C)。另外,骨髓间充质干细胞(MSCs)在稳定血管方面也发挥着功能作用。
在微流控器件中,生物力学因素是流体通过微流控通道或细胞外基质(ECM)产生的不同应力。剪切力是主要的生物力学因素,它高度依赖于流体流动。研究发现,剪切应力通过降低血管通透性以及降低血管壁厚度来增强屏障功能。对于EC内衬,EC在剪切力作用下被拉长并与流动方向对齐(图1(Aii))。此外,剪切应力能够通过一氧化氮(NO)信号刺激减弱HUVEC的入侵,这不受间隙流方向和VEGF梯度的影响。
间隙流是调节体内外细胞行为的另一重要因素,其对EC的作用力可促进毛细血管的形成。在体内,0.1–1 μm/s范围内的间隙流可刺激血管形成。在微流控装置中,流速如果在1.7–11 μm/s范围内,并伴随着较大的Péclet数(Pe>10),无论间隙流方向如何,都可刺激血管生成(图1(Ai))。这里Péclet数为对流与扩散传输的比率。对于血管新生,在与逆着间隙流方向上,从已有的血管网络中生成新血管的行为更加明显。研究发现,从基底到顶端的跨内皮流动可以触发EC从静止表型向侵袭表型的转变,从而生成血管。
除了流体力外,凝胶渗透率、孔径、纤维直径和硬度、降解速度等ECM力学性能在调节血管生成中也发挥了重要作用。胶原蛋白(collagen)和纤维蛋白(fibrin)是最常用的天然水凝胶,其力学性能可以灵活微调。胶原的力学性能可通过改变温度或pH的变化来调节,纤维蛋白的力学性能可通过改变纤维蛋白原和凝血酶浓度来调节。结果发现,与软凝胶相比,较硬的凝胶会产生直径较小的血管腔,血管芽结构在硬胶原凝胶中的侵袭程度明显降低(图1(Aiii))。此外,ECM内的纤维排布也会影响血管分布。除了这些被动机械应力外,施加在ECM上的主动机械应力对血管也会产生影响。例如,浮动的支架会使血管随机定向分布。然而,单向结构上的循环拉伸会使血管呈对角生长,而静态拉伸使血管呈垂直形生长。
2)细胞外信号分子
生长因子是细胞分泌的物质,它能够刺激细胞生长、增殖和分化。VEGF作为最重要的生长因子,能够通过VEGF受体-2信号调节EC的迁移和增殖。研究发现,较低浓度(2.5–5 ng/ml)的VEGF可诱导EC出芽。负VEGF梯度会诱导类似血管扩张的过程,而正VEGF梯度可诱导血管芽生成。除VEGF外,其他血管生成生长因子如血管生成素1(Ang-1)、转化生长因子β1(TGF-1)和碱性成纤维细胞生长因子(bFGF)可通过内皮尖端细胞丝状伪足从低浓度向高浓度梯度引导血管生成,并形成良好的排列。因此,生长因子的浓度梯度对于组织血管化至关重要(图1B)。这可以通过将含有成纤维细胞的海藻酸钠球体或包裹生长因子的微粒嵌入水凝胶中以产生局部浓度梯度来实现,或者通过微流控装置灌注含有生长因子的细胞培养基来实现。与作用于血管网络的单一生长因子相比,多种生长因子的组合会提高血管密度和稳定性。此外,通过调节流速和设计不同的微流控结构,可以构建不同梯度的生长因子。除了生长因子的空间效应外,VEGF浓度的时间变化也会影响血管生成。研究发现,与恒定剂量的血管内皮生长因子相比,高浓度的血管内皮生长因子的初始梯度随着时间的推移逐渐降低,可诱导生成理想的血管芽。因此,生长因子的释放、组合、剂量、梯度分布以及合适的作用时间都将促进血管的形成和稳定。
除生长因子的直接影响外,氧张力也会影响VEGF的分泌。缺氧环境中分泌的缺氧诱导因子(HIF)-1可启动VEGF的转录,这在诱导抗凋亡蛋白的表达,尤其是在肿瘤血管生成等病理性血管生成模型中起着重要作用。利用微流控可产生所需的氧气微环境,比如,由于PDMS的透气性高,通入不同浓度的气体、注入气体平衡培养液、氧清除操作或生成化学物质可以灵活创造缺氧微环境和氧张力梯度。此外,通过组合低透气热塑性塑料,能抑制外部微环境的干扰,从而增强了对PDMS热塑性混合微流控装置的氧气控制。
3)细胞源与细胞之间的作用
EC是组织血管形成的主要细胞。HUVEC由于其相对简单的分离方法被广泛应用于体外血管构建。不过当需要特异性EC时,需要使用其他EC来源来代替HUVEC。此外,诱导多能干细胞(iPSCs)衍生的EC已成为个性化药物研究的新内皮细胞来源。为了在体外建立成熟稳定的血管网络,需要将内皮细胞与壁细胞(如成纤维细胞、周细胞或MSCs)共培养。成纤维细胞可以合成并维持必要的基质蛋白(如I型胶原),分泌各种血管生成生长因子,以促进EC生成血管芽并形成管腔。此外,在稳定新形成的血管方面,在毛细血管和大血管(如小动脉、动脉、小静脉和静脉)周围的周细胞和平滑肌细胞(SMCs)也发挥着重要作用(图1C)。另外,骨髓间充质干细胞(MSCs)在稳定血管方面也发挥着功能作用。